Todo elemento químico possui propriedades comuns que se encaixam na Tabela Periódicas e essas são chamadas de propriedades periódias que são elas:
- RAIO ATÔMICO - É a distância entre o centro do núcleo e a Camada de Valência (camada mais externa do átomo). Na Tabela os elementos que se encontram mais a esquerda e mais abaixo são os que possuem maior Raio Atômico.
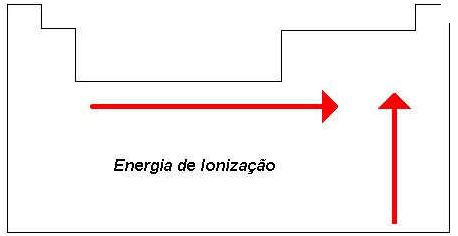
- ENERGIA DE IONIZAÇÃO - É a energia empregada para se retirar em elétron de um átomo. Na Tabela Periódica os elementos que estão mais a direita e mais acima são os que possuem maior energia de ionização.
- VOLUME ATÔMICO - É o volume ocupado por 1 mol de átomos no estado sólido. A representação na Tabela corresponde aos átomos presentes nos extremos.
- AFINIDADE ELETRÔNICA- Energia liberada para acrescentar elétrons no estado gasoso. Nesta relação a família dos Gases Nobres não possui essa propriedade.

- ELETRONEGATIVIDADE - Força com que os átomos atraem elétrons numa ligação química. Nesta relação a família dos Gases Nobres não possui essa propriedade.
- POTÊNCIAL DE IONIZAÇÃO - Energia para retirar um elétron de um átomo no estado gasoso.

- REATIVIDADE QUÍMICA - É a facilidade de realizar uma Ligação Química.
POR RAPHAELA SALES
ESTUDANTE DE ENGENHARIA QUÍMICA